Sirion사의 Lentivirus 제작서비스는 다음과 같은 장점을 제공합니다.
- 렌티바이러스 전문가의 프로젝트별 개인 컨설팅 및 기획
- 원하는 transgene DNA의 integration을 위한 수준높은 엔지니어링 서비스
- 신뢰할 수 있는 배치 간 일관성을 위한 표준 보장
- R&D에서 GMP 준비까지 모든 단계에 맞는 다양한 스케일 및 순도
- 맞춤형 QC 패키지
- GMP 제조 과정으로의 원활한 이전을 위한 CDMO 네트워크
Lentivirus Engineering
Lentivirus는 single stranded RNA genome을 가진 retrovirus 입니다. viral capsid와 matrix protein에 필요한 gag, viral integration과 GOI의 transcription에 필요한 pol, 숙주세포로의 진입에 필요한 env를 코딩하는 3가지 주요 유전자와 transgene DNA 삽입을 위한 recombinant lentivirus vector로 구성됩니다.
제3세대 Lentivirus vector는 virus genome의 대부분을 별도의 패키징 plasmid로 옮겨서 3'SIN (self-inactivating, 자체불활성화) 기술을 사용합니다. 3'UTR의 U3 영역에서 400bp가 결실되어 promotor가 비활성화 됩니다. 바이러스 DNA가 숙주 게놈에 통홥되는 동안 이 3'SIN LTR이 5'말단으로 전달되어 양 말단에서 U3 promotor 활성이 결여된 provirus가 생성됩니다. 따라서 3'SIN 기술은 내부 promotor로부터 제어된 유전자 발현을 가능하게 합니다. GOI를 운반하는 plasmid외에도 3'SIN 기술에는 LV 패키징 및 감염성 바이러스 입자 생성에 필요한 모든 단백질 구성 요소를 제공하기 위해 3개의 packaging plasmid가 필요합니다. Lentivirus vector는 virus envelop와 숙주세포의 융합을 매개하기 위해 VSV-G 단백질을 pseudotyping 합니다.
Figure 1: Schematic representation of the lentiviral vector genome organization. In the expression plasmid, viral cis-elements are removed and replaced with the gene of interest (GOI), promoter, and selection marker. To manufacture lentivirus vectors, three packaging plasmids are mixed together with the expression plasmid.
Constitutive Lentiviral vectors
Constitutive lentiviral vector는 dividing 및 non-dividing cell 모두 감염시킬 수 있으며 long-term으로 유전자를 발현하거나 silencing 할 수 있습니다. 또한 강력한 ubiquitous promoter (예, CMV, Ubc, EF1a 등)를 다양하게 제공하고 custom promoter를 도입할 수 있습니다. 다양한 selection marker (Puro, Neo, Blasti등)를 이용하고, bicistronic vector에 대한 IRES나 2A 시퀀스를 도입할 수 있고, 다양한 세포에 적용하기 위한 VSV-G를 pseudotyping 합니다.

Figure 2: Schematic representation of a constitutive lentiviral vector construct for cell model generation. Promoter and resistance can be selected based on experimental needs.
Inducible TET lentiviral vectors
Tet-system (Tetracycline-Controlled Transcriptional Activation)은 doxycycline (Dox) 항생제를 사용하여 효율적이고 가역적이며 제어 가능한 유전자 발현을 유도합니다. Tet-On 및 Tet-Off 벡터는 관심 있는 유전자를 제어하는 유도성 promoter와 함께 doxycycline-responsive transactivator protein gene을 가집니다. Tet-On system은 Tet-Off system보다 더 빠르게 Dox에 반응합니다.
Sirion의 Tet All-in-ONE은 최신 3G TET-On 기술을 사용하여 이 두 유전자를 단일 벡터에 제공합니다. GOI의 크기가 올인원 벡터의 삽입 기능을 초과하는 경우에도 두 벡터 시스템을 이용하여 유도 가능한 large construct를 전달할 수 있습니다.
Inducible vector 적용
- Stable inducible cell model generation
- Circumvention of cell adaption to stable genetic modification
- Characterization of toxic gene modulations
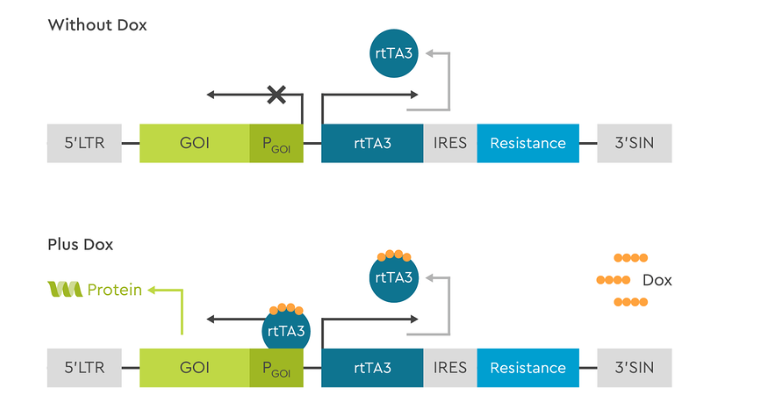
Figure 3: Schematic representation of the 3G Tet-On All-in-ONE system. In absence of Doxycycline in the medium, the transactivator protein rtTA3 is constitutively expressed but cannot bind to the promoter driving transcription of the GOI to activate it. When Doxycycline is added to the medium, it binds to rtTA3 and modifies its conformation, allowing it to bind to the promoter and activate transcription of GOI.
Tet All-in-ONE inducible vectors의 장점
- 유도 세포 발현 수준 300~400배 증가
- 백그라운드에서 10,000배 이상의 유도
- 고감도 및 활동성을 위한 개선된 디자인 : 기존 Tet-On보다 100배 적은 Dox를 사용하고 7배 더 많은 활동을 생성
- 최대 4kb 패키징 용량
- Clonal selection 과정 필요 없음
- Primary cell에 적합
- 고역가로 제조 가능
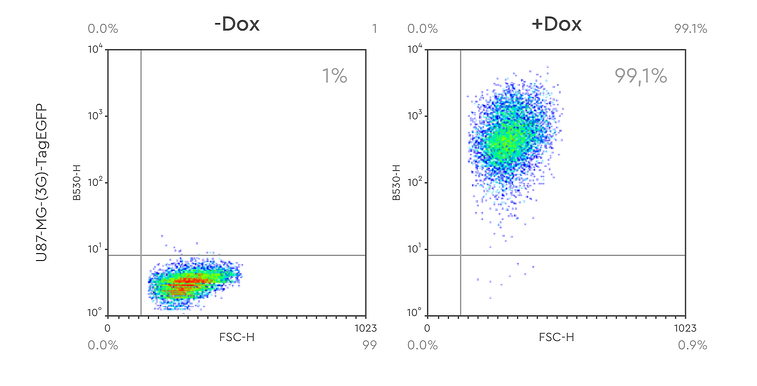
Figure 4: FACS analysis of stable U87MG cell pools with Tet-inducible expression of Tag-eGFP. Around 99% of the cells express Tag-eGFP when induced with Doxycycline.
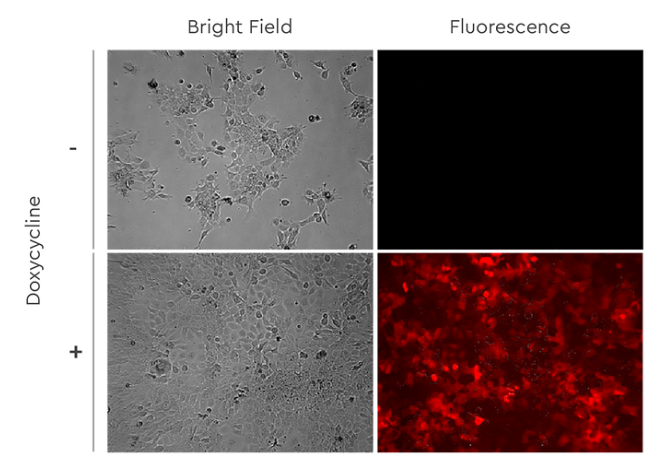
Figure 5: Fadu cells stably transduced with lentiviral vectors for inducible expression of RFP. Imaging after 48h in medium with or without 1,0 µg/ml Doxycycline.
Lentivirus QC
|
STANDARD
QC METHOD |
DESCRIPTION |
| Physical genomic particle titer (GC/ml) |
Viral RNA is lysed and prepared using the QIAamp®
Viral RNA Mini Kit from QIAGEN. The genomic titers are titrated against a
standard curve included in the Lenti-X™ qRT-PCR Titration Kit. |
| Functional titer (IU/ml) |
Relative expression level of the vector transgene is
measured by qRT-PCR relative to a control virus and a reference gene (hTOP1). |
| TU titer (TU/ml) |
The calculation is based on an average GC/TU quotient
of 10.2 which was determined experimentally using the LentiX provirus kit
(from Clontech) from > 200 individual determinations. |
| OPTIONAL QC METHOD |
DESCRIPTION |
| Endotoxin test |
Endosafe-nexgen-PTS Spectrometer |
| Functional testing in HEK293 cells |
Antibiotic selection, fluorescence detection,
luciferase measurement |
| Functional testing in custom cells |
Antibiotic selection, fluorescence detection,
luciferase measurement |
| Sterility test |
Incubation in CASO-Bouillon (Heipha) |
| Mycoplasma test |
PCR-based assay |
| TU titer (TU/ml) |
Determined experimentally using the LentiX provirus
kit (from Clontech) |
Lentivirus 서비스 종류
1) Constitutive Lentivirus 제작
| LV
CONSTITUTIVE PRODUCTION |
| SCALE |
SERVICE TYPE |
TIMELINES |
| >3E6-1E7 IU |
STANDARD |
3-4
weeks |
| >3E7-1E8 IU |
MEDIUM |
3-4
weeks |
| Lentiviral vector productivity evaluation |
|
3-4
weeks |
| >5E8 IU |
LARGE |
5-6
weeks |
| >1E9 IU |
X-LARGE |
6-7
weeks |
| >2.5E9 IU |
XX-LARGE |
6-8
weeks |
2) Inducible Lentivirus 제작
| LV
INDUCIBLE PRODUCTION |
| SCALE |
SERVICE TYPE |
TIMELINES |
| >3E6-1E7 IU |
STANDARD |
3-4
weeks |
| >3E7-1E8 IU |
MEDIUM |
3-4
weeks |
| Lentiviral vector productivity evaluation |
|
3-4
weeks |
| >5E8 IU |
LARGE |
5-6
weeks |
| >1E9 IU |
X-LARGE |
TBD |